
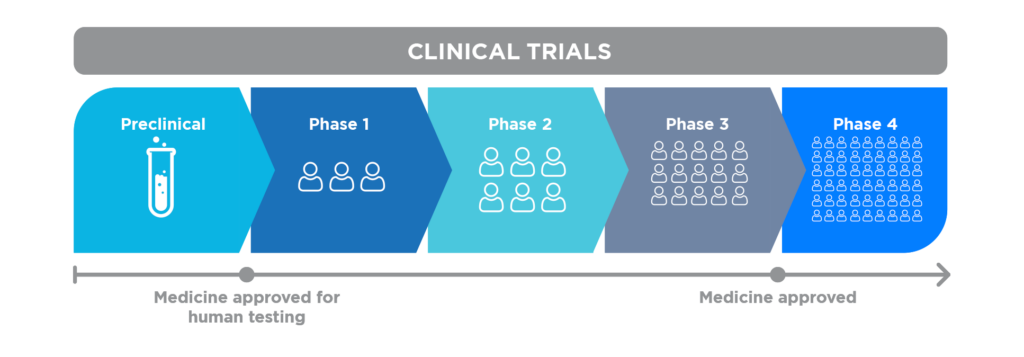


Questo processo è diventato più complesso nel tempo, coinvolgendo diverse aree aziendali e l'esternalizzazione di alcune attività alle Contract Research Organizations (CRO), spesso situate in molti paesi diversi.
Forniamo ampi servizi di consulenza GMP per aiutare i nostri clienti a stare al passo con le esigenze e le aspettative delle autorità di regolamentazione.
Esplora la nostra vasta libreria di audit GMP per vedere la gamma e la portata dei report live che abbiamo in magazzino, unisciti a un audit live o commissiona un audit su misura
Mantieni elevati standard di qualifiche dei fornitori di produzione di scienze biologiche e audit GMP all’interno della catena di fornitura attraverso la nostra esperienza
Scopri come possiamo aiutare il tuo prodotto a raggiungere il mercato, rispettando pienamente e dimostrabilmente i più recenti standard GxP
Dall’integrità dei dati all’implementazione di nuovi sistemi, il nostro team esperto con una mentalità digitale può guidarti verso risultati trasformativi
SEDE CENTRALE REPHINE
REPHINE BARCELONA S.L.U
REPHINE CINA
REPHINE INDIA