
Heutzutage müssen sich viele Unternehmen neuen Herausforderungen und Situationen stellen, die sich aus neuen Geschäftsmöglichkeiten ergeben: die Entwicklung eines neuen Produkts, die Eröffnung neuer Märkte in neuen Ländern oder geografischen Gebieten, Vereinbarungen mit internationalen Unternehmen für ein Projekt auf globaler Ebene… Dies führt zu der Notwendigkeit, neue oder andere Vorschriften einzuhalten, die zuvor nicht berücksichtigt wurden.
Die Öffnung für andere Märkte, sei es in Europa, den USA, im asiatisch-pazifischen Raum, im Nahen Osten oder in Lateinamerika, erfordert die Einhaltung hoher cGMP-Standards und den Erfolg bei den anschließenden Inspektionen, eine Voraussetzung für die Genehmigung neuer Aktivitäten oder Produkte.
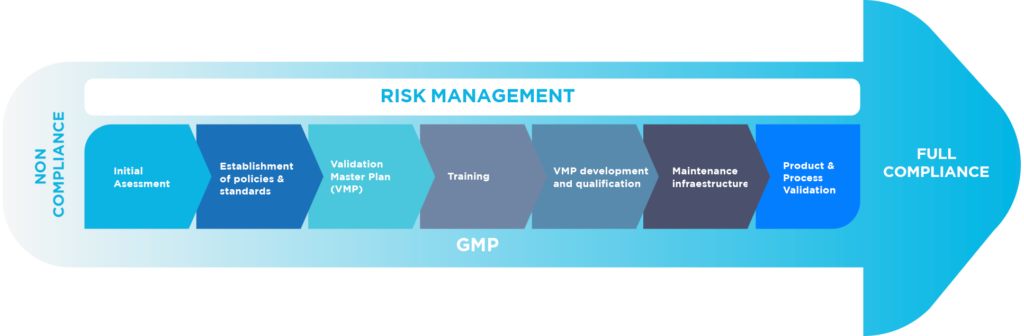


.

Anlagen, Geräte und kritische Versorgungseinrichtungen sowie Analyseinstrumente wurden gemäß den aktuellen Industriepraktiken und regulatorischen Anforderungen qualifiziert und validiert.
Wir bieten umfassende GMP-Beratungsdienstleistungen an, um unseren Kunden zu helfen, den Bedürfnissen und Erwartungen der Aufsichtsbehörden immer einen Schritt voraus zu sein.
Durchsuchen Sie unsere umfangreiche GMP-Auditbibliothek, um das Spektrum und den Umfang der Live-Berichte zu sehen, die wir auf Lager haben, nehmen Sie an einem Live-Audit teil oder beauftragen Sie ein massgeschneidertes Audit
Erhalten Sie hohe Standards für die Qualifizierung von Herstellern von Life-Science-Produkten und GMP-Audits innerhalb der Lieferkette durch unser Fachwissen
Entdecken Sie, wie wir Ihrem Produkt helfen können, den Markt zu erreichen und dabei vollständig und nachweislich die neuesten GxP-Standards einzuhalten
Von der Datenintegrität bis zur Implementierung neuer Systeme kann Sie unser erfahrenes Team mit einer digitalen Denkweise zu transformativen Erfolgen führen
REPHINE CHINA
REPHINE INDIA
Nach einem strengen Zertifizierungsverfahren durch Sparta verfügen wir über ein leistungsstarkes und erfahrenes Team, das TrackWise-Systeme gemäß den Anforderungen der einzelnen Kunden implementiert. Diese Anforderungen werden in verschiedenen Workshops erfasst und anschließend Prototypen erstellt.
Nach einem strengen Zertifizierungsverfahren durch Sparta verfügen wir über ein leistungsstarkes und erfahrenes Team, das TrackWise-Systeme gemäß den Anforderungen der einzelnen Kunden implementiert. Diese Anforderungen werden in verschiedenen Workshops erfasst und anschließend Prototypen erstellt.