
Oggigiorno, molte aziende devono affrontare nuove sfide e situazioni derivanti da nuove opportunità commerciali: lo sviluppo di un nuovo prodotto, l’apertura di nuovi mercati in nuovi paesi o aree geografiche, accordi con aziende internazionali per un progetto su scala globale… Ciò si traduce nella necessità di rispettare normative nuove o diverse, non considerate in precedenza.
L’apertura ad altri mercati, in Europa, Stati Uniti, Asia-Pacifico, Medio Oriente o America Latina, richiede la necessità di conformarsi a standard elevati di cGMP e il successo nelle successive ispezioni, un prerequisito per l’approvazione di nuove attività o prodotti.
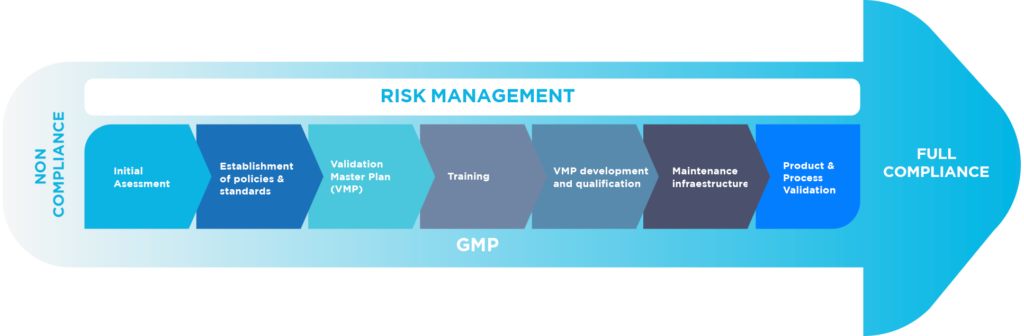


.

Strutture, apparecchiature e utenze critiche, strumenti analitici sono stati qualificati e convalidati secondo le attuali prassi del settore e i requisiti normativi.
Forniamo ampi servizi di consulenza GMP per aiutare i nostri clienti a stare al passo con le esigenze e le aspettative delle autorità di regolamentazione.
Esplora la nostra vasta libreria di audit GMP per vedere la gamma e la portata dei report live che abbiamo in magazzino, unisciti a un audit live o commissiona un audit su misura
Mantieni elevati standard di qualifiche dei fornitori di produzione di scienze biologiche e audit GMP all’interno della catena di fornitura attraverso la nostra esperienza
Scopri come possiamo aiutare il tuo prodotto a raggiungere il mercato, rispettando pienamente e dimostrabilmente i più recenti standard GxP
Dall’integrità dei dati all’implementazione di nuovi sistemi, il nostro team esperto con una mentalità digitale può guidarti verso risultati trasformativi
SEDE CENTRALE REPHINE
REPHINE BARCELONA S.L.U
REPHINE CINA
REPHINE INDIA
Dopo un rigoroso processo per ottenere la certificazione da Sparta, disponiamo di un team potente ed esperto per implementare i sistemi TrackWise in base alle esigenze di ciascun cliente. Questi requisiti vengono acquisiti attraverso diversi workshop e vengono realizzati prototipi successivi.
Dopo un rigoroso processo per ottenere la certificazione da Sparta, disponiamo di un team potente ed esperto per implementare i sistemi TrackWise in base alle esigenze di ciascun cliente. Questi requisiti vengono acquisiti attraverso diversi workshop e vengono realizzati prototipi successivi.