
La validation des procédés doit être comprise, au-delà des traditionnels « trois lots consécutifs », comme la preuve documentée d’une solide connaissance scientifique et d’une compréhension du procédé, en tenant compte des paramètres critiques du procédé et de la manière dont ils affectent les attributs de qualité, les risques sur le produit et le procédé, et les mécanismes de contrôle mis en place pour leur prévention tout au long de leur cycle de vie.
Les produits développés selon une approche de la qualité par la conception (QbD), où la stratégie de contrôle du processus peut être définie de manière scientifique et exhaustive, la fabrication en continu peut être utilisée et, ensuite, la vérification continue du processus peut remplacer l’approche de validation traditionnelle.

De l’initiative de la FDA en 2002 sur « l’approche basée sur les risques » à nos jours, et avec l’entrée en vigueur des nouvelles directives de la FDA (2011), de l’EMA (2014) et de la mise à jour de l’annexe 15 des BPF de l’UE, des changements importants ont été apportés à la validation des processus de fabrication.
En fait, l’approche en « trois étapes », soulignant l’intégration de l’étape de vérification continue des processus (UE) ou de vérification continue des processus (FDA) et la pertinence accordée au traitement statistique des données de processus et de produits, modifie radicalement les méthodologies et les approches pour répondre à cette exigence essentielle des BPF.
L’objectif principal devient de s’assurer en permanence que le processus reste dans un état de contrôle adéquat pendant la fabrication commerciale des lots, ainsi que de faciliter l’identification des changements nécessaires dans la stratégie de contrôle afin de favoriser l’amélioration continue des produits et des processus.
À cette fin, un programme de collecte et d’analyse des données de processus et de produits et de leur qualité continue doit être mis en place.

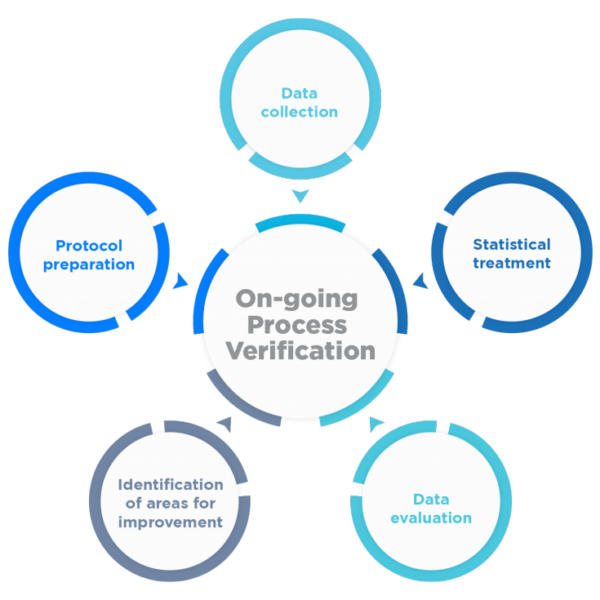
Rephine possède une vaste expérience au niveau international en matière de validation des processus, soutenue par de nombreux projets et des inspections réussies de nos clients par les autorités sanitaires européennes et la FDA (inspections de pré-approbation/régulières), notamment :
SIÈGE SOCIAL DE REPHINE
REPHINE BARCELONA S.L.U
REPHINE CHINE
REPHINE INDE