Affrontare le sfide normative: la tua guida alla presentazione del DMF in Cina
Orientarsi nel mercato farmaceutico cinese non è facile, soprattutto quando si tratta di registrazione di API ed eccipienti. Per vendere in Cina, le aziende devono presentare un Drug Master File (DMF) alla National Medical Products Administration (NMPA), un processo noto per le sue complessità normative, le esigenze amministrative e le barriere linguistiche.
Comprendere il processo DMF in Cina
La presentazione di un DMF implica più della semplice trasmissione di un file tecnico. I produttori stranieri devono nominare un agente locale, una filiale o un rappresentante registrato, per gestire la presentazione e tutte le comunicazioni correlate con il Centre for Drug Evaluation (CDE) e NMPA.
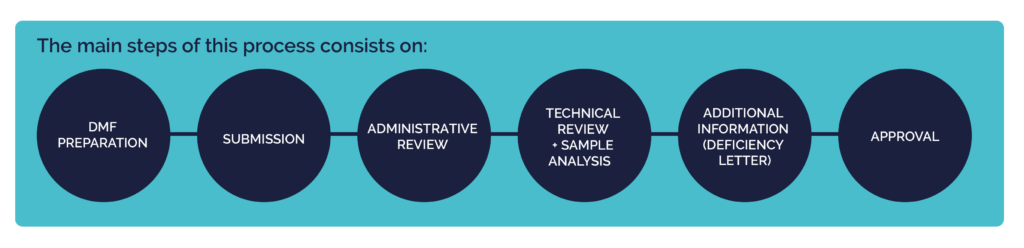
I passaggi principali includono:
- Revisione del DMF esistente per la conformità alle linee guida cinesi.
- Traduzione di tutta la documentazione in cinese.
- Gestione delle attività amministrative, inclusa la registrazione come agente ufficiale e la preparazione di pacchetti di documenti completi.
- Gestione delle lettere di carenza del CDE e garanzia di risposte tempestive.
- Coordinamento della spedizione dei campioni richiesti e garanzia che tutte le richieste di dati aggiuntivi siano soddisfatte.
Senza competenza locale, ritardi, incomprensioni e fallimenti di conformità possono facilmente far deragliare il processo.

Perché Rephine?
Rephine colma il divario tra le aziende farmaceutiche internazionali e il mercato cinese. Con uffici in Europa e a Shanghai, combiniamo gli standard globali con il know-how locale, garantendo che il processo si svolga senza intoppi salvaguardando al contempo la riservatezza delle informazioni.
I nostri servizi includono:
- Assistenza normativa e tecnica completa per le presentazioni DMF.
- Agire come agente ufficiale per la gestione amministrativa.
- Gestione di tutte le comunicazioni con CDE e NMPA, comprese le traduzioni.
- Garantire la conformità alle normative cinesi in evoluzione.
Il comprovato processo di presentazione DMF di Rephine
Successo nel mondo reale: superare gli ostacoli normativi - Un caso di studio
Uno dei clienti internazionali di produzione di API di Rephine ha dovuto affrontare sfide significative con la presentazione del proprio DMF in Cina. Dalle barriere linguistiche alle sfumature normative, il processo è sembrato scoraggiante.
Rephine ha fornito supporto end-to-end, conducendo una revisione dettagliata della conformità del DMF esistente, garantendo l’allineamento con le linee guida cinesi e la farmacopea cinese. Hanno gestito le traduzioni, si sono registrati come agente ufficiale presso l’NMPA e hanno gestito tutti i processi amministrativi, dalla presentazione della documentazione alle risposte alle lettere di carenza. Gli sforzi rapidi e coordinati di Rephine hanno portato a un’approvazione DMF tempestiva e di successo, consentendo l’accesso al mercato.
Panreac Química, un produttore globale leader di eccipienti, ha elogiato la competenza di Rephine:
“La competenza, la professionalità e la profonda comprensione dei requisiti normativi di Rephine sono state fondamentali per il nostro successo.” — Panreac Química


