시운전 및 적격성 평가 방법론은 장비 및 서비스 공급업체, 담당 엔지니어링 부서, 그리고 시설의 엔지니어링 부서와의 협력 작업에 기반을 둡니다.

이는 우수한 운영 절차, 방법, 지침, 훈련된 인력, 그리고 공정에 관련된 장비, 시설 및 서비스의 적절한 적격성 평가를 의미합니다.
위험 관리 방법론(ICH Q9)에 따라 수행되는 적격성 평가는 각 적격성 평가 대상 요소의 중요 측면에 집중하고 동시에 시간과 자원을 최적화하기 위해, 장비 및 공정 환경에 대한 지식과 통제의 필수적인 증거를 제공하는 핵심 요소입니다.
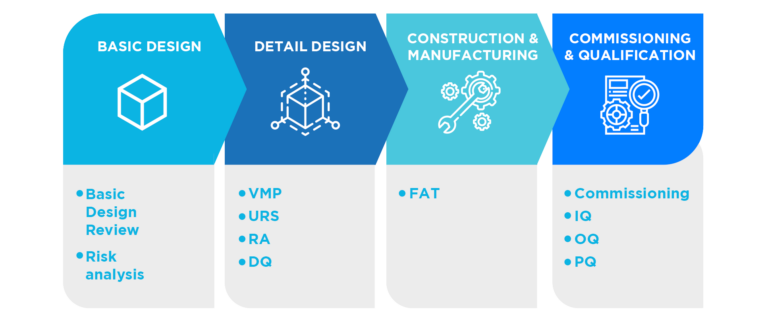
이러한 방식으로, 당사는 고객이 GMP 규정 준수 목표를 달성하는 데 필요한 경험과 지식을 제공합니다. 설계, 시운전 및 적격성 평가 단계에서 말입니다. 또한, 당사는 유효성 검증 활동을 통해 프로젝트에 품질을 통합하고, 품질 표준 및 적격성 평가 문서를 표준화하며, 엔지니어링 부서의 자원을 최적화합니다.

당사는 고객이 규제 기관의 요구 사항과 기대를 앞서 나갈 수 있도록 광범위한 GMP 컨설팅 서비스를 제공합니다.
당사의 광범위한 GMP 감사 라이브러리를 탐색하여 보유하고 있는 실시간 보고서의 범위와 규모를 확인하고, 실시간 감사에 참여하거나, 맞춤형 감사를 의뢰하십시오.
REPHINE 중국
REPHINE 인도